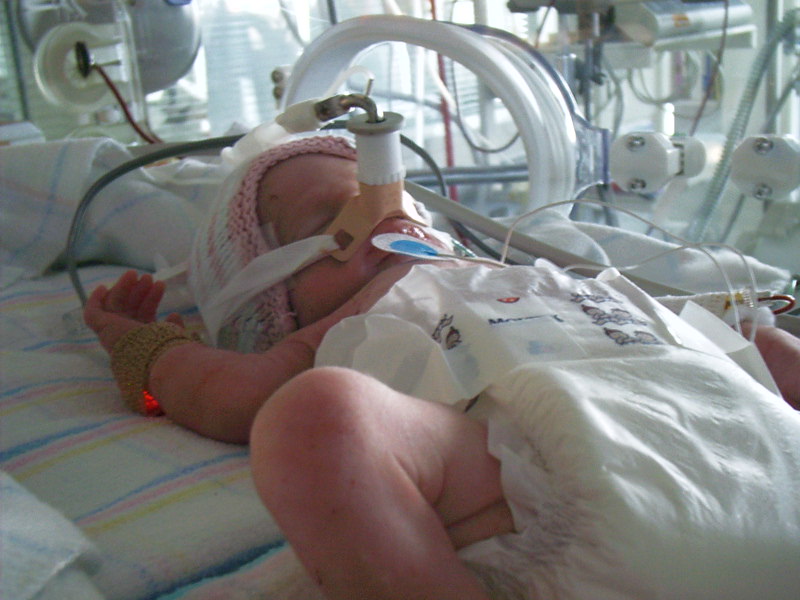
 El medicamento, conocido como Makena (caproato de hidroxiprogesterona), reduce el riesgo de parto prematuro que, según los expertos, incrementa el riesgo de problemas para el bebé en el momento del nacimiento, de discapacidades para toda la vida como parálisis cerebral e incluso de muerte.
El medicamento, conocido como Makena (caproato de hidroxiprogesterona), reduce el riesgo de parto prematuro que, según los expertos, incrementa el riesgo de problemas para el bebé en el momento del nacimiento, de discapacidades para toda la vida como parálisis cerebral e incluso de muerte.
Los partos prematuros son un problema grave en los EE. UU. Comenta Shelly Burgess, vocera de la FDA.
El parto prematuro, antes de completar la semana 37 de embarazo, afecta a 1 de cada 8 bebés nacidos en los EE. UU.
El índice de nacimientos prematuros ha aumentado en más de 35 % en los últimos 25 años en los EE. UU., mientras que los partos prematuros tardíos, es decir, entre las semanas 34 y 36, corresponden a cerca de las tres cuartas partes de esos nacimientos. El medicamento Makena reducirá el riesgo de parto prematuro antes de la semana 37 de gestación en mujeres embarazadas que tengan antecedentes de parto prematuro espontáneo.
Agregó que Makena está aprobado para un cierto subgrupo de mujeres estadounidenses que están en riesgo de parto prematuro: las que van a tener un solo bebé (embarazo simple) que anteriormente ya han dado a luz prematuramente.
El objetivo del medicamento no es su uso en mujeres que van a tener gemelos ni que tengan otros factores de riesgo para parto prematuro. El factor de riesgo más común para el embarazo prematuro es la reincidencia, confirma el Dr. Alan Fleischman, vicepresidente principal y director médico de March of Dimes. Este es el primer medicamento aprobado para prevenir la reincidencia en mujeres que han tenido un parto simple prematuro y ahora tienen un solo bebé.
El caproato de hidroxiprogesterona no ha estado exento de controversias. En 2006, un comité asesor de la FDA que estaba considerando el fármaco para el tratamiento del parto prematuro encontró motivos para cuestionar su seguridad, como una posible relación con abortos espontáneos en el segundo trimestre.
Según la agencia, el caproato de hidroxiprogesterona es el mismo medicamento que antes se llamaba Delautin, que la FDA aprobó en 1956 y se usaba para tratar perturbaciones hormonales femeninas y cáncer, y fue retirado del mercado por razones comerciales en 2008. Makena es químicamente igual a Delautin, asegura un funcionario de la FDA.
El Dr. Gene Burkett, profesor de ginecoobstetricia de la facultad de medicina de la Universidad de Miami aseguró que se trata de algo que se ha estado usando con las mujeres propensas al parto prematuro. Ha sido casi el estándar de cuidado por los últimos cinco o seis años. Makena fue aprobado según las regulaciones de aprobación acelerada de la FDA, que permiten que medicamentos promisorios sean aprobados por mostrar beneficios clínicos reales. Parte de los términos para la aprobación exigen que el fabricante realice estudios que demuestren que el fármaco ofrece beneficios.
Para tomar su decisión, la FDA revisó datos sobre la seguridad y la efectividad de Makena a partir de un ensayo clínico en el que participaron 463 mujeres embarazadas que tenían antecedentes de partos prematuros espontáneos.
El estudio de confirmación que estan haciendo irá seguido por otro similar de seguimiento con bebés que se completará en 2018. Se espera que en ese estudio participen entre 580 y 750 bebés, según la cantidad de centros y de mujeres que deseen participar, señala la FDA.
Makena se administra por inyección una vez a la semana entre las semanas 16 y 37 del embarazo. Se trata de una forma sintética de una hormona que se produce durante el embarazo.
Entre los efectos secundarios se encuentran dolor, inflamación o picazón en el lugar de la inyección, urticaria, náuseas y diarrea, según la FDA. Las reacciones adversas graves son poco comunes, aunque hubo un informe sobre un coágulo en los pulmones y otro de infección en el lugar de la inyección.